合作单位:Jiangxi Normal University
魔德科技:帮助客户研究异槲皮素与卵清蛋白的分子识别以及荧光淬灭机制
参考文献: Food Chemistry. 2020, 309, 125667. DOI: 10.1016/j.foodchem.2019.125667 (IF = 6.306 一区top期刊)
背景
卵清蛋白(OVA)是一种球状蛋白质,与其他可食用蛋白质相比,具有更高的营养价值、发泡能力、乳化性能和抗氧化能力,因此被广泛用于食品制造行业。但是,在食物的加热加工过程中,OVA可能会发生糖化反应,蛋白质的糖基化可以增强蛋白质的功能特性,但也可以诱导一些有害的糖基化产物生成,如AGEs、丙烯酰胺等。
研究表明,糖基化抑制剂可以一定程度上缓解蛋白质的糖基化并减少AGEs生成。黄酮类化合物具有较强的抗糖基化能力,但目前尚未有异槲皮素抗糖基化活性的研究。
方案设计
鉴于目前异槲皮素抗糖基化的作用机制仍不明确,因此本研究主要采用光谱-质谱方法研究异槲皮素抑制OVA糖基化的作用机制。为了深入研究异槲皮素与OVA的分子识别,经与魔德科技(www.modekeji.cn)技术团队沟通,拟采用分子模拟方法从原子层面获得异槲皮素与OVA的复合物结构,并从分子结构方面分析异槲皮素抗糖基化的机理。
主要结果
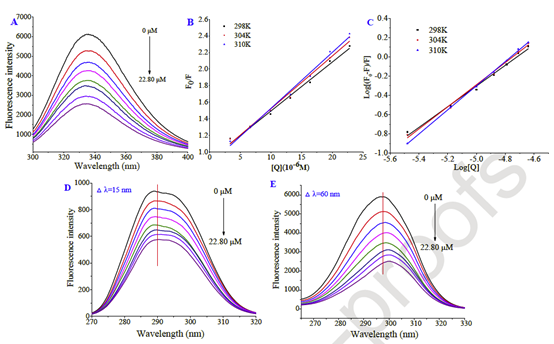
本文首先分别检测了不同浓度的异槲皮素对OVA荧光强度的影响,结果表明异槲皮素对OVA蛋白的荧光具有较强的淬灭作用。
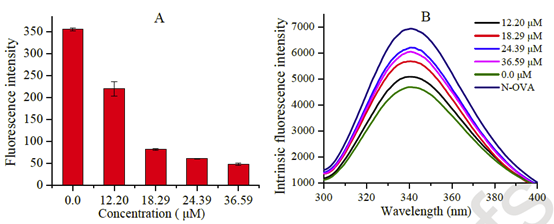
图2 分析了异槲皮素的结合对OVA的荧光的影响,结构表明异槲皮素可以影响OVA蛋白荧光生色团附近的微环境。通过同步荧光分析可以发现,异槲皮素主要是影响了OVA蛋白中的酪氨酸和色氨酸附近的极性,进而使蛋白整体荧光淬灭。
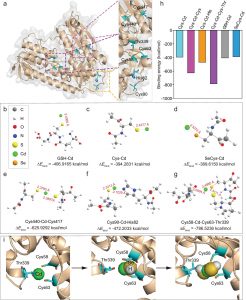
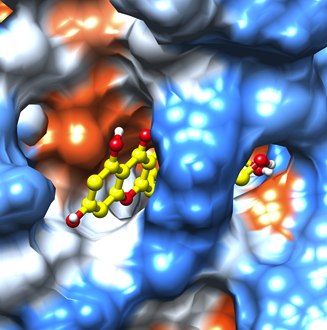
经与魔德科技技术团队沟通商量,本文拟采用分子对接方法来研究异槲皮素和OVA蛋白的结合模式,进一步分析异槲皮素使蛋白荧光淬灭的主要作用机制,对接结果如图3-4所示。从图中可以看出,异槲皮素主要结合在蛋白的疏水性空腔内部,并与周围的氨基酸形成了较强的氢键和疏水相互作用,还可以与Y125形成π-π堆积作用。
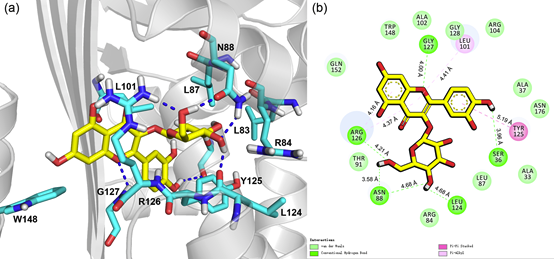
通过分子模拟可以发现,氢键,范德华力和疏水作用是异槲皮素与OVA分子识别的重要结合力,这也进一步验证和补充了前面的热力学分析结果。
拓展知识
ECD计算方法:首先优化化合物基态的分子结构,计算从基态到一批激发态的激发能和振子强度,然后根据这两个量用高斯函数展宽,即可以得到化合物的紫外-可见吸收(UV-Vis)光谱,若用转子强度代替振子强度进行展宽,则可以得到ECD光谱。