合作单位: Hainan University
参考文献:Yuge Hou, Ying Li, Wensi Huang, et al. Journal of Chromatography A, 2020, 1632:461609-. DOI:10.1016/j.chroma.2020.461609(IF= 4.601)
用合成的片状聚吡咯(ppy)纳米线作为固相萃取材料,采用气相色谱-质谱联用技术对人血浆中拟除虫菊酯类农药的痕量残留进行了检测。建立并验证了一种测定人血浆中痕量拟除虫菊酯(跨氟菊酯、丙烯菊酯、异氰菊酯、甲氰菊酯、乙醚菊酯、氰戊酸酯)多残留方法。实验结果表明,该方法可作为复杂生物样品中拟除虫菊酯类农药痕量残留分析的有效检测方法。对拟除虫菊酯类杀虫剂的临床监测和毒理学研究具有一定的指导意义。
背景:
在农药中,拟除虫菊酯类杀虫剂以其高效、作用迅速、广谱、光稳定性强等优点在世界范围内广泛应用于农业害虫的防治。然而,拟除虫菊酯类农药对动植物有害,对环境、农业生产和经济也会造成严重影响。研究表明,拟除虫菊酯中毒可造成基因损伤、细胞损伤、神经损伤、生殖损伤等危害。中毒的主要机制是影响电压门控钠离子通道。因此,有必要建立适当的富集和分析方法来监测拟除虫菊酯类杀虫剂的使用情况。然而,以往的检出拟除虫菊酯的方法存在操作复杂、耗时等缺陷。
ppy作为一种常见的导电聚合物,因其良好的环境稳定性和对极性化合物的萃取能力而得到广泛应用。目前常用的ppy纳米线合成方法有软模板法、硬模板法和无模板法。研究表明,由于氢键、π-π相互作用和疏水相互作用等相互作用,ppy纳米线可以作为吸附剂应用于固相萃取(SPE)。到目前为止,大多数研究都集中在拟除虫菊酯在环境、蔬菜和水果中的残留。血浆中拟除虫菊酯残留的检测和标准的建立很少。因此,本研究合成ppy纳米线作为固相萃取吸收剂,用于人体血浆样品中痕量拟除虫菊酯类农药的测定,用于临床监测和毒理学研究。
方案设计:
采用SEM、TEM、FT-IR、XRD、TGA等实验对ppy进行表征。采用分子动力学模拟(Molecular dynamics, MD)方法研究了ppy纳米线与拟除虫菊酯的吸附机理。考察并优化了提取条件,包括洗脱液类型、洗脱液用量、提取时间和ppy纳米线用量。由于对聚吡咯结构与6种不同菊酯类化合物的吸附情况以及吸附过程尚不清楚,经与魔德科技(www.modekeji.cn)技术团队沟通,采用分子动力学模拟(Molecular Dynamics, MD)来研究聚吡咯对菊酯类化合物的吸附情况。
主要结果:
本研究以阳离子表面活性剂十六烷基三甲基溴化铵(CTAB)为软模板,通过氧化聚合法制备了具有规则形貌的ppy纳米线。采用扫描电镜(SEM)、透射电镜(TEM)、x射线衍射分析(XRD)、傅里叶变换红外光谱(FT-IR)、热重分析(TGA)等技术进行了表征。6种拟除虫菊酯的检出限为0.008 ~ 0051 ng mL−1,定量限为0.028 ~ 0.162 ng mL−1。ppy纳米线的相对标准偏差为2.12 ~ 5.09%,6种拟除虫菊酯的回收率为76.9 ~ 110.4%。富集因子范围为47.09 ~ 51.30。采用分子动力学方法模拟了拟除虫菊酯和ppy纳米线的吸附机理。基于密度分析、分子识别分析和结合能分析,认为范德华力是拟除虫菊酯类化合物和ppy纳米线吸附的重要驱动力。
MD模拟结果分析
分别提取MD模拟前后6个体系的构象,如图1所示。从图中可以看出,Transfluthrin, Allethrin, Resmethrin, Fenpropathrin, Edeltamethrin和Fenvalerate经过MD模拟均能吸附在聚吡咯纳米材料的表面。其中Fenpropathrin与聚吡咯表面的吸附效果相对较差,Fenpropathrin分子在溶液中自组装成球,因此限制了其与聚吡咯表面的结合。

密度分布
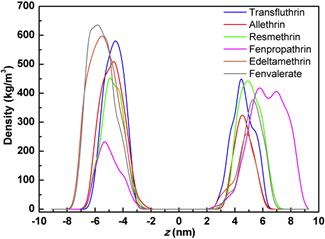
为了进一步分析模拟体系中菊酯类分子的紧密程度,分别对6个体系中菊酯类化合物沿盒子的密度分布进行了分析。如图2所示,从图中可以看出,除Fenpropathrin外,菊酯类化合物主要分布在距离盒子中心2~6 nm的范围内,最大密度均在400 kg/m3以上,表明这些分子可以较为紧密地分布在聚吡咯表面。而Fenpropathrin在聚吡咯表面的分布范围达到了盒子的边缘,表明其在聚吡咯表面的分布相对较分散。
分子识别研究
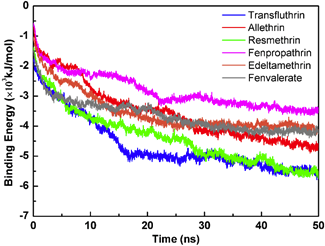
为了进一步研究菊酯类化合物与聚吡咯的亲和力以及结合的驱动力,本文对二者的结合能进行了计算和分析。如图3所示,6种菊酯类化合物都可以与聚吡咯纳米材料结合,结合能在-6000 ~ -3000 kJ/mol范围内,其中Transfluthrin和Resmethrin与聚吡咯的亲和力相对最强,而Fenpropathrin的亲和力相对较弱。
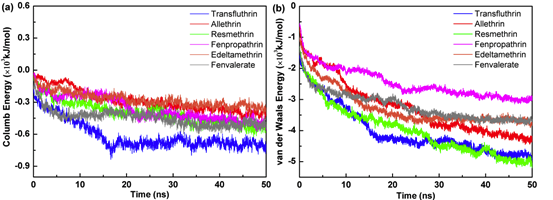
结合能分为库伦作用项和范德华作用项,为了研究各个能量项对结合能的贡献大小,图4分别给出了两个能量项的作用力大小。从图4中可以看出,库伦作用力大小范围在-300~-600 kJ/mol,而范德华作用大小在-5000~-3000 kJ/mol 范围。因此,范德华相互作用的能量贡献是菊酯类化合物与聚吡咯分子识别的主要驱动力。
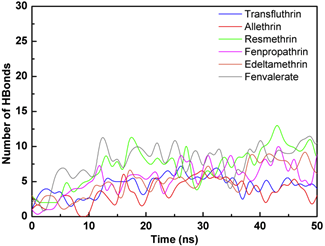
菊酯类化合物结构中均含有氢键受体,因此氢键作用可能对其吸附过程有一定的促进作用。图5给出了6种菊酯类化合物与聚吡咯的氢键数量变化,从图中可以看出,菊酯类化合物与聚吡咯的氢键作用并不强,平均每个菊酯分子形成的氢键在0.05~0.1个,因此氢键作用并不是菊酯类化合物吸附到聚吡咯表面的关键作用力。